

 Задачи с решениями
Задачи с решениями

Кристаллическая решетка железа при комнатной температуре – кубическая объемноцентрированная. Атомы железа расположены в вершинах куба и в центре – на пересечении пространственных диагоналей куба. Сколько атомов железа приходится на одну элементарную ячейку? Определите постоянную решетки (ребро куба)
Каждый атом железа, находящийся в вершине куба, принадлежит одновременно восьми ячейкам. Таких атомов восемь. Кроме того, в центре куба расположен еще один атом, принадлежащий только данной элементарной ячейке. Таким образом, на элементарную кубическую объемноцентрированную ячейку приходится
Объем
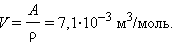
Число элементарных ячеек в объеме одного моля
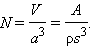
Так как на каждую элементарную ячейку приходится
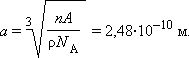
 1 из 2
1 из 2
 |
Главная Бесплатные онлайн учебники Бесплатная подготовка по всем предметам онлайн |
||
|
© Физикон, 1999-2026 E-mail: |
||
|
|
||