Глава 3. Молекулярная физика и термодинамика Задачи с решениями
Задачи с решениями

Рассчитайте изменение энтропии при нагревании m = 1 кг воды от температуры T1 = 300 К до температуры T2 = 360 К. Удельная теплоемкость воды в этом интервале температур постоянна и равна c = 4200 Дж/(кг·К).
РешениеДля вычисления изменения энтропии ΔS нужно рассмотреть процесс квазистатического нагревания воды, когда каждая последующая бесконечно малая порция теплоты dQ передается воде, находящейся в равновесном состоянии при некоторой температуре T, и вызывает бесконечно малое изменение температуры dT:
dQ = cmdT,
где c – удельная теплоемкость воды.
Следовательно,
Подстановка числовых значений дает:
ΔS = 0,76·103 Дж/К.
При нагревании воды энтропия увеличивается.
 1 из 2
1 из 2
 |


 Задачи с решениями
Задачи с решениями

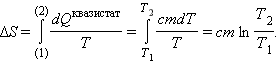
 1 из 2
1 из 2
